突破课堂教学中的难点,是教学活动中永恒的主体。教师应根据教材的需求,运用各种教学方式,设计出适合学生的教学过程,学生才能积极主动地学习,突破教学难点。
一、运用实验探究法,突破教学难点
教师先根据教学内容和学生的认知水平、实验能力,创设情境,提出问题,再让学生自己通过实验探究、推理分析、对假说进行检验和修正、得出结论。
在《苯》这部分内容中,苯分子结构是教学难点,学生可以通过实验探究与讨论来认识其结构。1.提出假设:从分子式(C6H6)看,它应含有碳碳不饱和键,所以苯能使溴水或酸性KMnO4溶液褪色。2.实验验证:①向少量的苯中加入溴水,振荡,现象是溶液分层,下层溶液变浅,上层呈橙红色。②向少量的苯中加入酸性KMnO4溶液,振荡,现象是溶液分层,下层为紫红色,上层为无色。3.结论:苯不能使溴水或酸性KMnO4溶液褪色。凯库勒式表示法是不确切的。4.讨论、小结:1.苯分子里6个键完全相同,是一种介乎于单键和双键之间的独特的键。2.2个原子都在同一平面上,苯分子具有平面正六边形结构。3.为了表示苯分子的结构特点,结构简式用■表示。
运用实验探究法,教师不仅可以顺理成章地突破教学难点,而且培养了学生的科学素质和综合能力。
二、善用故错艺术,突破教学难点
教师可以根据以往的经验,在貌似严格的步骤中、在貌似严密的推理中,巧妙地把学生中常见的典型错误展现出来。
例:将PH=8的NaOH溶液和PH=10的NaOH溶液等体积混合,求混合液的PH值。教师可以先给出错误的解法:
∵PH=8的NaOH溶液中[H+]=10-8mol/L, PH=10的NaOH溶液中[H+]=10-10mol/L
∴混合液中[H+]=■≈■×10-8mol/L,PH=-lg[H+]=-lg1/2×10-8mol/L≈8.3。学生发现这种解法与自己解法的不同,由此引起了一场激烈的争论。最后师生共同得出:碱溶液混合,应根据混合前后OH-物质的量不变来计算。
∵PH=8的NaOH溶液中[OH-]=■mol/L=10-6mol/L
PH=10的NaOH溶液中[OH-]=■mol/L=10-4mol/L
∴混合液中[OH-]=■=■×10-4mol/L [H+]=■mol/L=2×10-10mol/L PH=-lg[H+]=-lg2×10-10mol/L=9.7
在这样的课中,教师越是一个不着痕迹的“败者”,就越是一个“胜者”,一个成功者。由此可见,故错艺术在教学中恰当运用,不仅可以集中学生注意力,激发和活化了学生的学习兴趣,还能培养多项思维能力。
三、精编口诀,突破教学难点
知识点多、生、杂是化学科的特点,学生对一些概念、反应原理难以深入理解。如果教师把这些难懂的概念和原理编成通俗易懂、平仄压韵的口诀,就可以起到事半功倍的效果。
对《化学平衡》中的难点:学会平衡图像的解题方法与技巧,教师就可以编成以下的口诀:1.视图:一看面二看线三看点四看辅助线五看量的变化;2.技巧:“先拐先平,数值大”;“定一议二”。
例:已知4NH3(g)+5O2(g)?圳4NO(g)+6H2(g). △H=-1025KJ/mol。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是( )
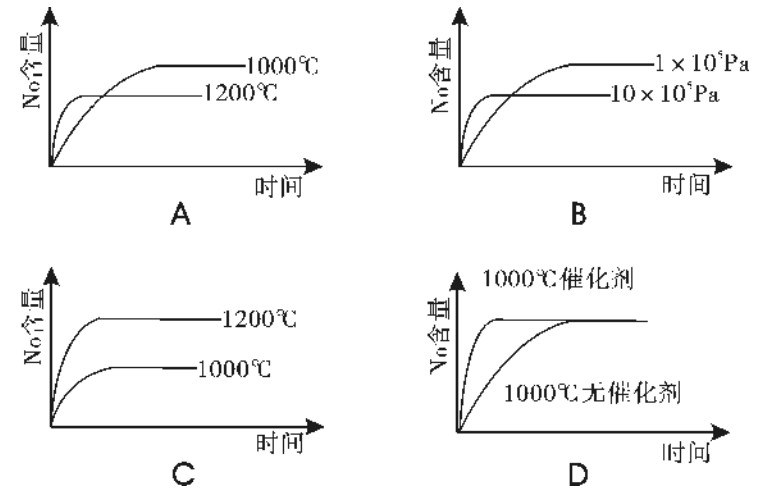
解析:根据“先拐先平,数值大”的口诀,选项A、B正确,因为根据升高温度,平衡向吸热反应方向移动;根据使用催化剂只能改变化学反应速率,缩短达到平衡的时间,但对化学平衡的移动无影响,所以选项D正确。【答案】C
类似这样的口诀,记忆时容易上口,使用起来方便快捷,很受学生的欢迎,能引起学生学习化学的兴趣,提高学习极积性,进而突破教学上的难点。
四、借助其它学科手段,突破教学难点
在课堂教学中,许多教学难点常常可以借助其它学科的相关知识和方法得以简捷快速地解决和突破,收到事半功倍的效果。
1.借助数学方法,突破教学难点
在化学教学中,我们经常要运用数学中的极端假设法、换元法、等效法等等来进行突破难点。《化学平衡》这部分理论性很强,也是教学难点,要求学生具备平衡的思想和很强的逻辑思维能力。在可逆反应中,各种物质只能在某一范围内变化,很难达到极限值100﹪或0。于是,当假设物质反应到一个极限值后,就可能产生一种特殊的解决问题的思路,这就是极端假设法。
例:在一密闭容器中进行反应:2SO2(g)+O2(g)?葑2SO3(g)。该反应某一时刻SO2、O2、SO3的浓度分别为0.2mol·L-1、0.1mol·L-1、0.2mol·L-1。当反应达到平衡时,可能存在的数据是( )
A. SO2为0.4mol·L-1,O2为0.2mol·L-1
B. SO3为0.25mol·L-1
C. SO2、SO3均为0.15mol·L-1
D. SO3为0.4mol·L-1
解析:采取极端假设法,先假设SO2和O2全部转化为SO3,此时,SO2和O2的物质的量浓度都是0,而C(SO3)=0.4mol·L-1,再假设SO3全部转化为SO2和O2,此时,SO2和O2的物质的量浓度分别是0.4mol·L-1,0.2mol·L-1,而C(SO3)=0,故三物质的浓度范围分别为:0<C(SO2)<0.4mol·L-1,0<C(SO3)<0.4mol·L-1,0<C(O2)<0.2mol·L-1,故选项A、C、D是不可能的。【答案】B
2.借助物理手段,突破教学难点
判断多原子分子是极性分子还是非极性分子是教学中的一个难点。教师可以借助物理学中的受力分析来突破。
如CO2:以碳原子为质点,两个氧原子为拉力,如图:■,由于两个氧与碳原子在同一直线上,两边的作用力相等(即F1=F2),方向相反,相互抵消,合外力为零,故CO2分子为非极性分子。通过以上的教学,学生自然总结出这样的结论:以中心原子为质点,对质点进行受力分析,合力为零者为非极性分子,合力不为零者为极性分子。
在教学过程,要突破课堂教学难点,教师除了认真钻教材,遵循学生的认知规律,还要采用恰当的教学方式,因材施教,这也是体现我们教师教学艺术之所在。只有这样,课堂教学中的难点才能得到突破。


